顶刊高光・辉煌里程碑
中乔新舟助力成果荣登国际顶刊,影响因子 42.5 再创新高!热烈祝贺!
l 文献标题:Hijacking ERAD for targeted degradation of transmembrane proteins
l 研究单位:复旦大学发表
l 期刊:CELL
l 影响因子:42.5

期刊名称:《CELL》
靶向蛋白降解(TPD)技术为药物发现提供了巨大机遇,但降解跨膜(TM)靶点仍然充满挑战。由于TM蛋白在内质网膜上规范地折叠,我们假设利用ER相关降解(ERAD)可能实现TM蛋白的高效降解。在此,我们建立了一种TPD技术,将其命名为ERAD结合嵌合体(ERADECs),能够高效降解TM靶点。我们鉴定了地奈德是SYVN1的结合剂,SYVN1是一种介导ERAD的ER E3连接酶。我们通过将去sonide与已知的PD-L1配体连接,设计了针对程序性死亡配体1(PD-L1)的ERADECs,并以高效能观察到SYVN1和ERAD依赖的PD-L1降解。在功能上,这些ERADEC在肿瘤抑制和PD-L1降低作用上表现得比临床使用的PD-L1抗体更为显著。ERADEC的概念也可扩展到其他膜靶点。我们共同建立了一种平台技术,利用ERAD以极高的效率选择性降解TM靶点。
我们荣幸地向长期使用中乔新舟细胞以及专用培养基的合作伙伴致以热烈祝贺由复旦大学研究团队完成的成果《Hijacking ERAD for targeted degradation of transmembrane proteins》发表于国际知名期刊《CELL》(IF=42.5)。在该研究中,作者团队选用了中乔新舟提供的A-375人恶性黑色素瘤细胞专用培养基(货号:ZM0042),NCI-H1975人肺腺癌细胞专用培养基(货号:ZM0395),MDA-MB-231人乳腺癌细胞(货号:ZQ0118),NCI-H1975人肺腺癌细胞(货号:ZQ0395),A375人恶性黑色素瘤细胞(货号:ZQ0042)用于关键细胞模型的培养。
A-375人恶性黑色素瘤细胞专用培养基(买二送一,三瓶到手678)
中乔新舟®货号:ZM0042
NCI-H1975人肺腺癌细胞专用培养基
中乔新舟®货号:ZM0395
A375人恶性黑色素瘤细胞(STR鉴定)
[细胞+500ml专培套餐促销]:980¥
中乔新舟®货号:ZQ0042
MDA-MB-231人乳腺癌细胞(STR鉴定)
[细胞+500ml专培套餐促销]:980¥
中乔新舟®货号:ZQ0118
NCI-H1975人肺腺癌细胞(STR鉴定)
[细胞+500ml专培套餐促销]:980¥
中乔新舟®货号:ZQ0395
本研究建立“一种劫持ERAD的TPD策略“,ERAD是一条关键的降解通路,能够通过多种不同途径降解TM蛋白、分泌蛋白或错误折叠的胞质蛋白。ERAD由内质网膜相关的E3连接酶(ER-E3)通过对目标蛋白的多泛素化(poly-Ub)启动。在多泛素化之后,底物被p97/VCP(含瓜氨酸蛋白)ATP酶转运到胞质区,并在提取过程中由p97/VCP结合的去泛素化酶(DUBs)去泛素化,然后底物重新被泛素化并靶向蛋白酶体降解。在TPD领域中,ERAD在很大程度上被忽视,并且此前没有利用ERAD劫持的TPD方法。团队假设,与ER-E3和目标蛋白同时相互作用的化学嵌合体可能通过ERAD触发选择性降解,这在TPD中尚未被利用。基于这一假设以及意外发现的可与主要ER-E3 SYVN1相互作用的化学配体,建立了一种劫持ERAD的TPD策略,称为ERAD-介导的嵌合体(ERADECs)。
研究团队最近确定地塞尼德(desonide)是一种针对亨廷顿病(Huntington’s disease)致病突变型HTT蛋白(mHTT)的小分子降解剂。地塞尼德诱导mHTT多泛素化(poly-Ub)以增强其降解,因此我们使用小干扰RNA(siRNA)敲低测试了可能直接与mHTT相互作用的多泛素化相关酶的潜在参与(图S1A和S1B)。这些酶的选择基于HDinHD数据库,并通过文献确认其在mHTT降解中可能的参与,这一作用通过地塞尼德诱导降低HEK293T细胞中外源表达的mHTT exon1 Q72片段来测量(图S1A)。敲低SYVN1完全抵消了地塞尼德处理对mHTT水平的下降,提示SYVN1的参与(图S1B),SYVN1是酵母Hrd1的哺乳动物同源物,也是ERAD中发挥主要作用的内质网E3。我们进一步通过测试mHTT的多泛素化证实了这一点,地塞尼德处理增强了多泛素化,而敲低SYVN1后这种效应几乎被阻断(图1A)。我们观察到地塞尼德诱导的高分子量血凝素(HA)条带增加,这与通过过表达泛素导致的mHTT多泛素化增加相对应(图S1C),从而确认地塞尼德诱导mHTT多泛素化。为了测试其潜在机制,我们进行了共免疫沉淀(coIP),观察到地塞尼德处理增强了mHTT与SYVN1的相互作用(图1B)。K6R突变(Q72K6R)对地塞尼德具有抗性,并且是已知的地塞尼德结合蛋白——糖皮质激素。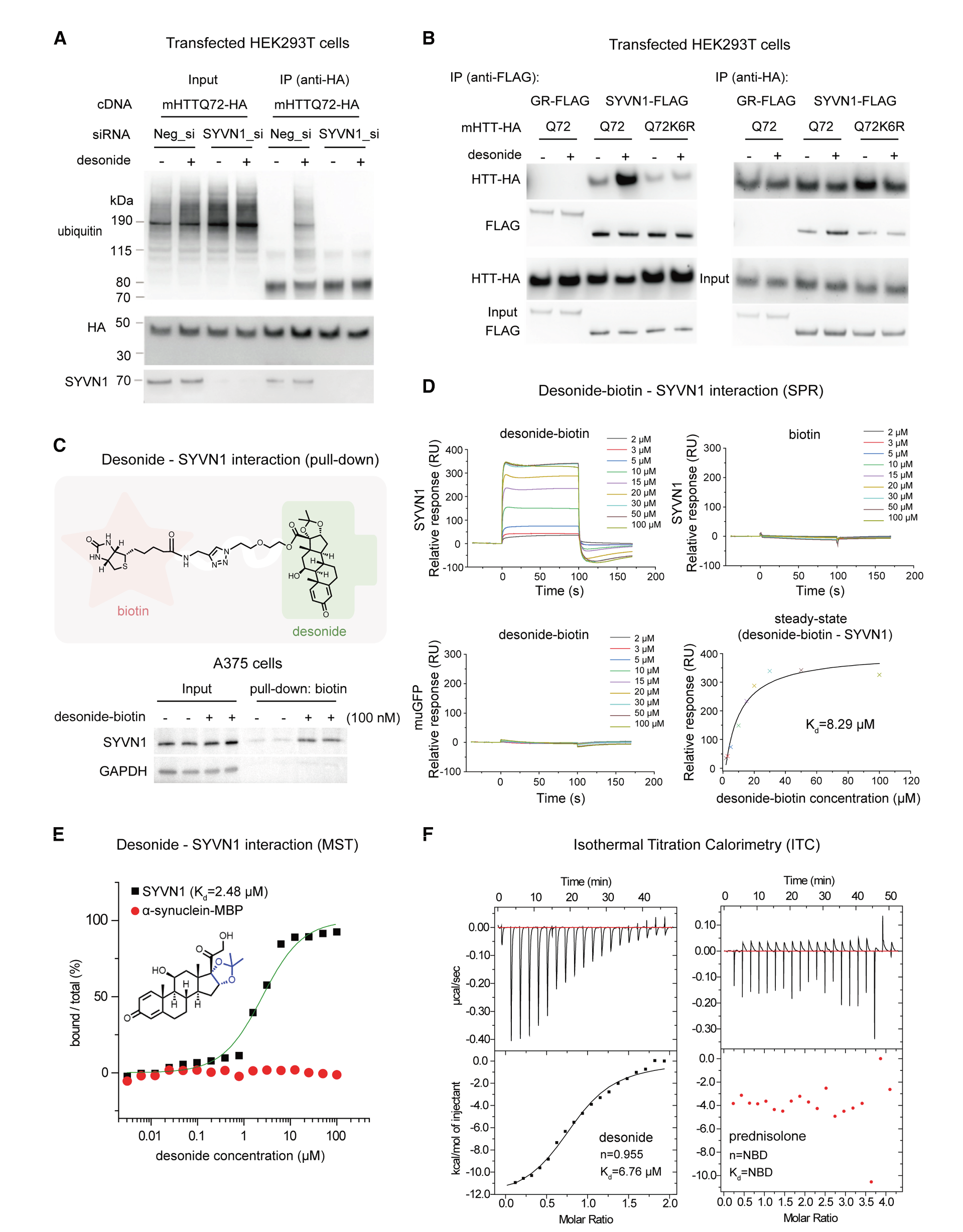
图1:地索奈德直接与SYVN1相互作用
l (A) 使用HEK293T细胞进行代表性免疫沉淀-西方印迹实验,这些细胞转染了所示的cDNA质粒(24小时)和siRNA(48小时),然后用3 μM地索尼德(+)或含100 nM环氧霉素联合处理的DMSO(-)对照处理24小时。
l (B) 使用HEK293T细胞进行代表性免疫沉淀-西方印迹实验,这些细胞转染了GR-FLAG、SYVN1-FLAG和mHTT-HA cDNA质粒(36小时),然后仅用3 μM地索尼德(+)或DMSO(-)对照处理2小时,以避免随后降解。
l (C) 代表性下拉实验,使用地塞米松-生物素(+)或生物素对照(-)与 A375 细胞孵育,通过西方印迹确认其与 SYVN1 的相互作用。
l (D) 使用重组纯化蛋白的代表性表面等离子体共振(SPR)检测结果显示,地塞米松-生物素而非生物素可直接与 SYVN1 相互作用。muGFP 蛋白被用作对照蛋白。
l (E) 类似于 (D),但使用 MST 测定法测试 desonide-SYVN1 相互作用。α-突触核蛋白-MBP 蛋白被用作对照蛋白。
l (F) 类似于 (E),但使用 ITC 测定法。在本图及以下图的所有 Western 印迹中,未裁剪的凝胶图像显示在 Data S1 中。
研究团队考虑将地塞米松连接到已知的TM蛋白靶点的配体/抑制剂上,以验证ERADEC的概念。通过比较地塞米松和其他保留或消除了SYVN1结合的GR激动剂的结构(图1E、1F、S1E和S1F),并考虑到将生物素连接到地塞米松的C-20位置并未破坏SYVN1结合(图1C),C-21羟基可能不是SYVN1结合所必需的,并可用于连接链接物以合成潜在的ERADEC。 因此,我们通过将地塞米松与PD-L1配体BMS-202连接(图2A),生成了靶向程序性死亡配体1(PD-L1)的ERADEC,并测试了它们对PD-L1水平的影响(图2B和2C)。值得注意的是,10种不同的靶向PD-L1的ERADEC(P-ERADEC P1–P4和P8–P13)在MDA-MB-231和A375细胞中以pM–nM浓度范围显著降低了PD-L1水平(图2B和2C;数据S2A和S2B)。然而,一些仅含柔性聚乙二醇(PEG)链接物的P-ERADEC(P5–P7)未能降低PD-L1(图2C;数据S2B)。大多数有效的含酯链接物的P-ERADEC表现出亚nM的DC50和>90%的Dmax,而含酰胺链接物的P-ERADEC P12和P13对细胞内水解更具抵抗力,其效力和效能类似(图2B和2C)。我们进一步通过流式细胞术分析完整A375细胞确认了质膜PD-L1水平的下降(图2D)。P2诱导的PD-L1下降相对较慢(超过12小时)(图2E),这可能是因为ERADEC主要直接降解靶蛋白的内质网池而非跨膜池。
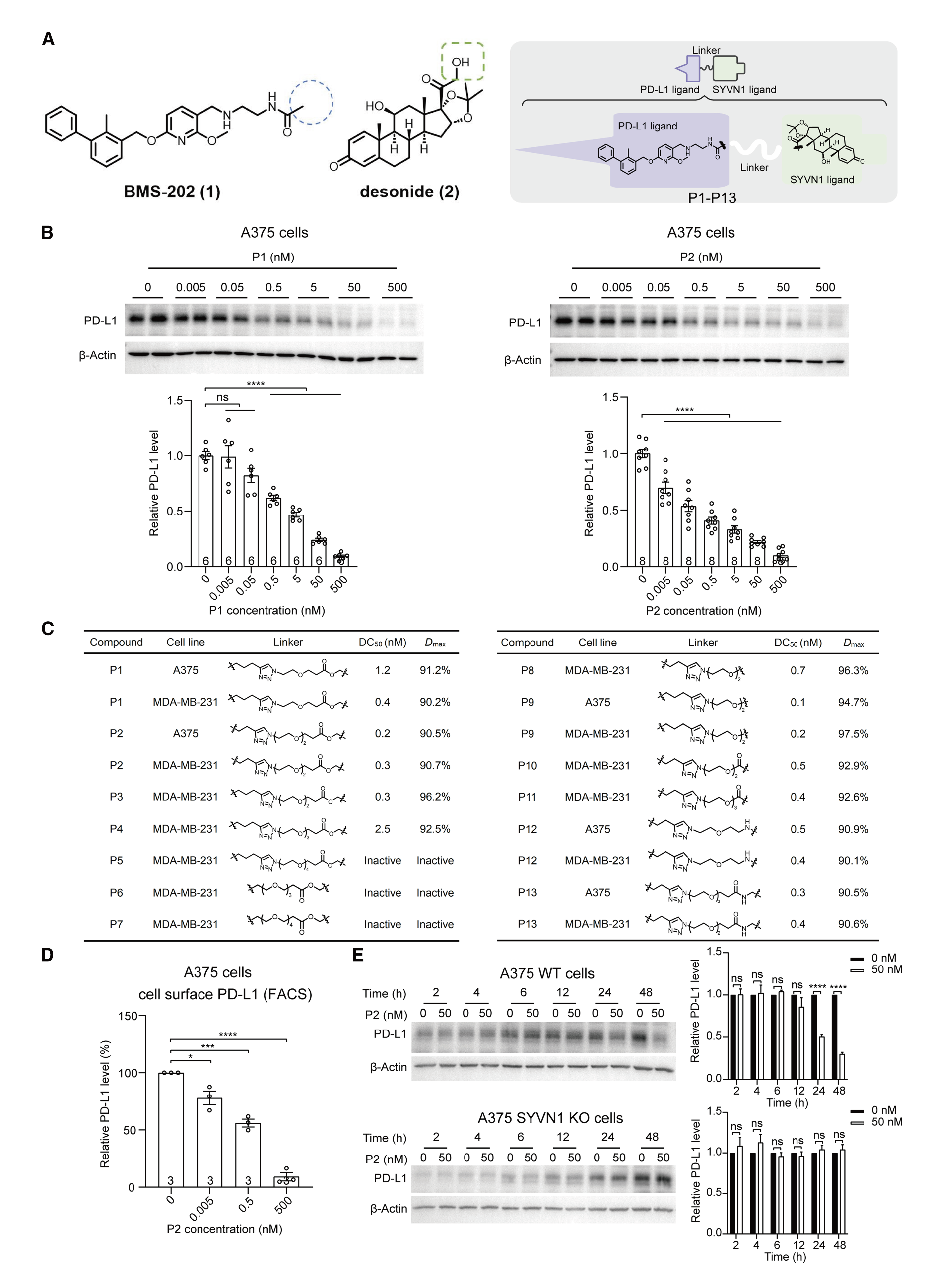
图2. 基于地塞米松的ERADECs降低A375细胞中的PD-L1蛋白水平
l (A) P-ERADECs 的化合物设计图和二维结构。
l (B) 使用 A375 细胞在分别用指定浓度的 P1 或 P2 处理 48 小时后的代表性西方印迹及定量结果。
l (C) P-ERADECs 的 PD-L1 DC50(半最大降解浓度)和 Dmax(最大降解)的表格
l (D) 用流式细胞术分析 A375 细胞在用指定浓度 P2 处理 48 小时后的质膜 PD-L1 蛋白水平。
l (E) 使用 A375 野生型(WT)细胞和 A375 SYVN1 敲除(KO)细胞,在有或没有 50 nM P2 处理不同时间(分别为 2、4、6、12、24 和 48 小时)下的代表性西方印迹及定量分析。所有柱状图表示平均值 ± SEM。ns,p > 0.05;*p < 0.05,**p < 0.01,***p < 0.001,****p < 0.0001
关于ERADECs特异性的一个担忧是,我们当前的弹头,它可以作用于SYVN1,同时也是一个GR激动剂。GR不太可能介导降解效应,因为使用另一种GR激动剂泼尼松龙的化合物未能引起靶标降解。
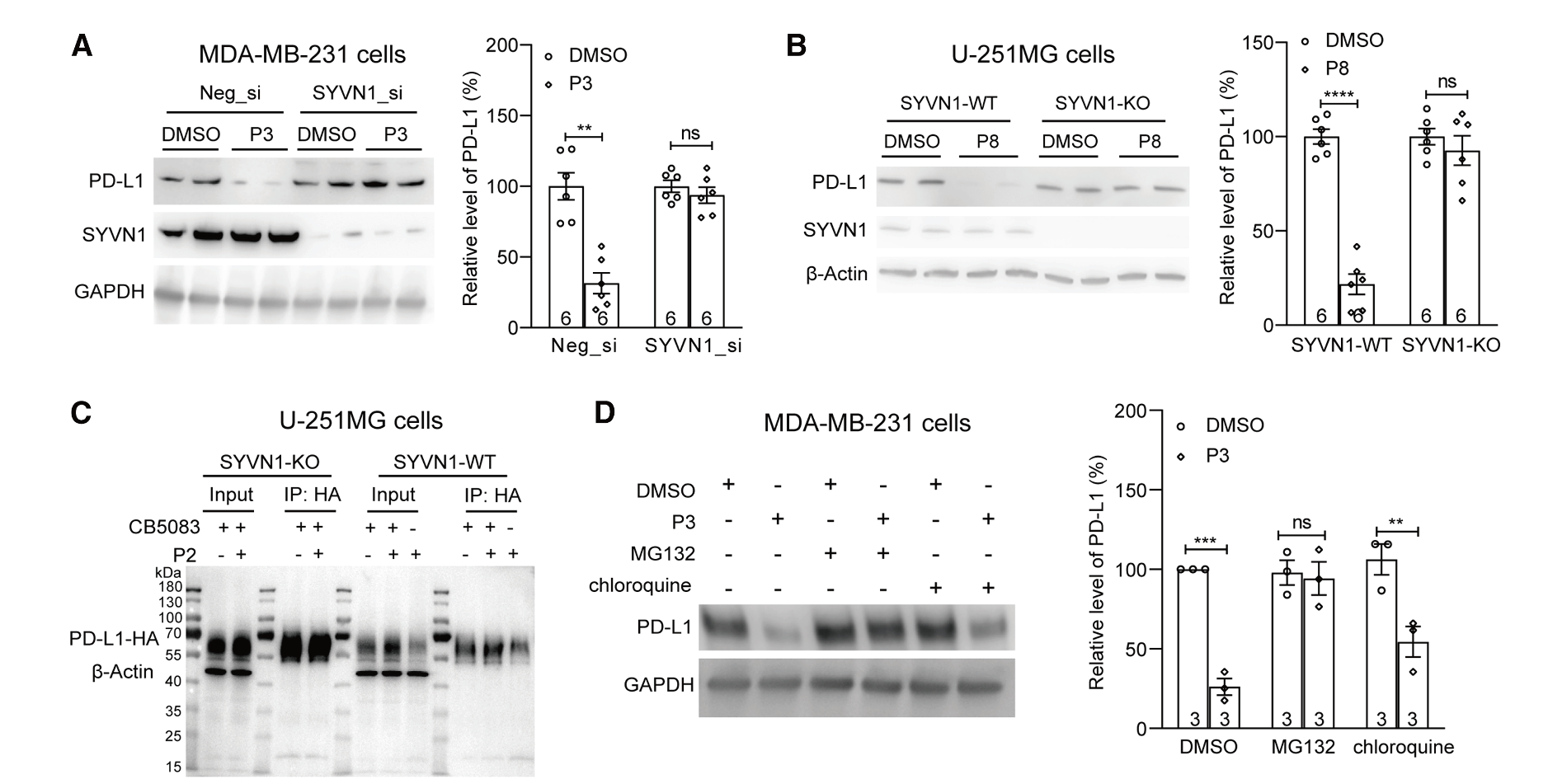
图3. ERADECs 通过 SYVN1 和 ERAD 降低 PD-L1 蛋白水平
l (A) 在 MDA-MB-231 细胞中转染所示 siRNA 48 小时后,再用 500 nM P3 或 DMSO 对照处理 24 小时,对 PD-L1 水平进行代表性免疫印迹及定量分析。
l (B) 类似于 (A),但使用 U-251MG 细胞,有或没有 SYVN1 基因敲除,处理 500 nM P8。
l (C) 使用转染表达 PD-L1-HA 和泛素质粒的 U-251MG 细胞进行代表性免疫共沉淀-免疫印迹及定量分析,以检测 P2 诱导的 PD-L1 多聚泛素化。A375 细胞用 50 nM P2 处理 6 小时以诱导多聚泛素化,并用 500 nM CB5083 处理以防止多聚泛素化 PD-L1 的降解。
l (D) MDA-MB-231 细胞用所示化合物处理 48 小时后进行代表性免疫印迹及定量分析。P3,500 nM;MG132,1 μM;氯喹 (CQ),20 μM。
鉴于KDM5B促进糖酵解,我们首先试图将这一代谢性状与下游信号传导联系起来。TCGA-PRAD数据集的GSEA显示,高KDM5B表达组中“通过切合体进行替代mRNA剪接”通路富集(ES = 0.6876,NP = 0.0000)。这促使我们假设KDM5B驱动的乳酸积累可能影响AR切割,从而产生抗性相关变异体AR-V7。支持这一观点的是,在我们的小鼠CDX模型中,KDM5B敲低细胞的肿瘤组织乳酸水平较低。当肿瘤组织接受乳酸处理时,AR-V7 mRNA水平随时间和剂量变化增加,确立乳酸与AR-V7表达之间的直接联系。
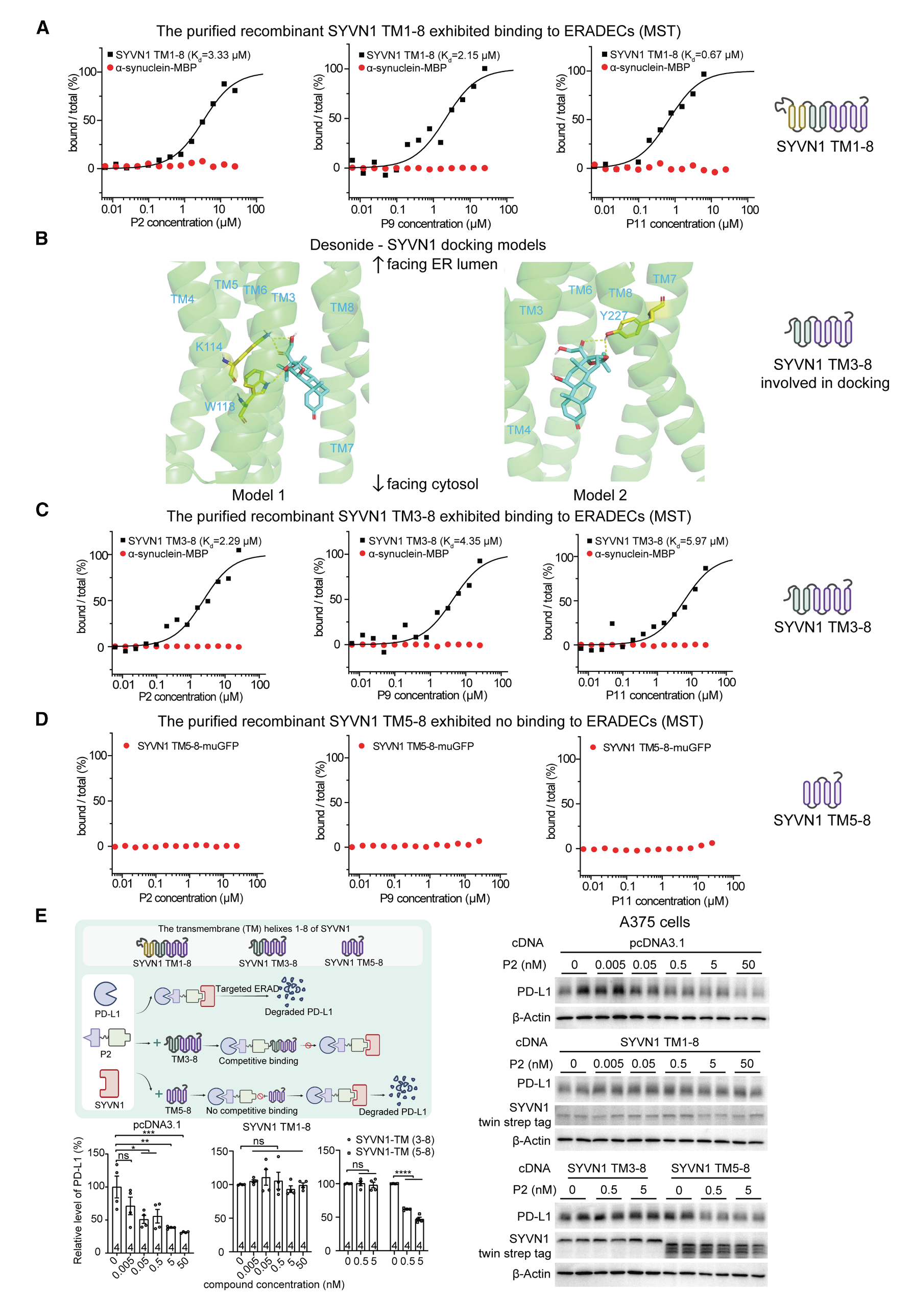
图4. P-ERADECs 可能结合在 SYVN1 的 TM 域中的 TM3–8 口袋处
l (A) 代表性 MST 实验结果显示,纯化的重组 SYVN1 TM1–8 域对所示的 P-ERADECs 表现出结合。
l (B) Desonide(碳原子显示为青色)与 SYVN1(碳原子显示为绿色)的前两个分子对接模型。图中显示了 TM 结构、氢键长度(埃)、以及参与的残基(碳原子显示为黄色)。
l (C 和 D) 类似于 (A),但使用所示的 SYVN1 TM 片段。
l (E) 使用过表达的 SYVN1 TM 片段进行竞争实验。对转染了所示质粒并在之后用 P2 处理 48 小时的 A375 细胞进行的 Western 印迹及定量分析证实了竞争现象。柱状图表示均值 ± SEM。ns, p > 0.05;*p < 0.05,**p < 0.01,***p < 0.001,****p < 0.0001。另见图 S4–S7
我们进一步基于模型1和模型2,通过LigPlot分析了可能与地索尼德相互作用的SYVN1氨基酸(图5A)。我们在一个构建体中(SYVN1-5mut)或在各自的单独构建体中进行预测参与地索尼德与SYVN1结合的关键氨基酸突变(E87A、W118F、Y227F、L250S和Q254A)(图5A),并在SYVN1敲除的U-251MG细胞中表达这些突变体或野生型(WT)全长SYVN1,以测试它们是否能够恢复P-ERADEC的作用。与模型1预测的结合位点不一致,但与模型2预测一致,将全长SYVN1表达在SYVN1 KO U-251MG细胞中恢复了P-ERADEC P2处理下PD-L1的下降作用,而表达Y227F突变体或5突变SYVN1形式则未能实现这一点(图5B、5C和S4E),将降解作用与化合物-SYVN1相互作用位点联系起来,进一步确认了SYVN1的参与。结合位点通过直接生物物理实验检测二元结合(通过MST和ITC)得到了进一步确认(图5D和5E)。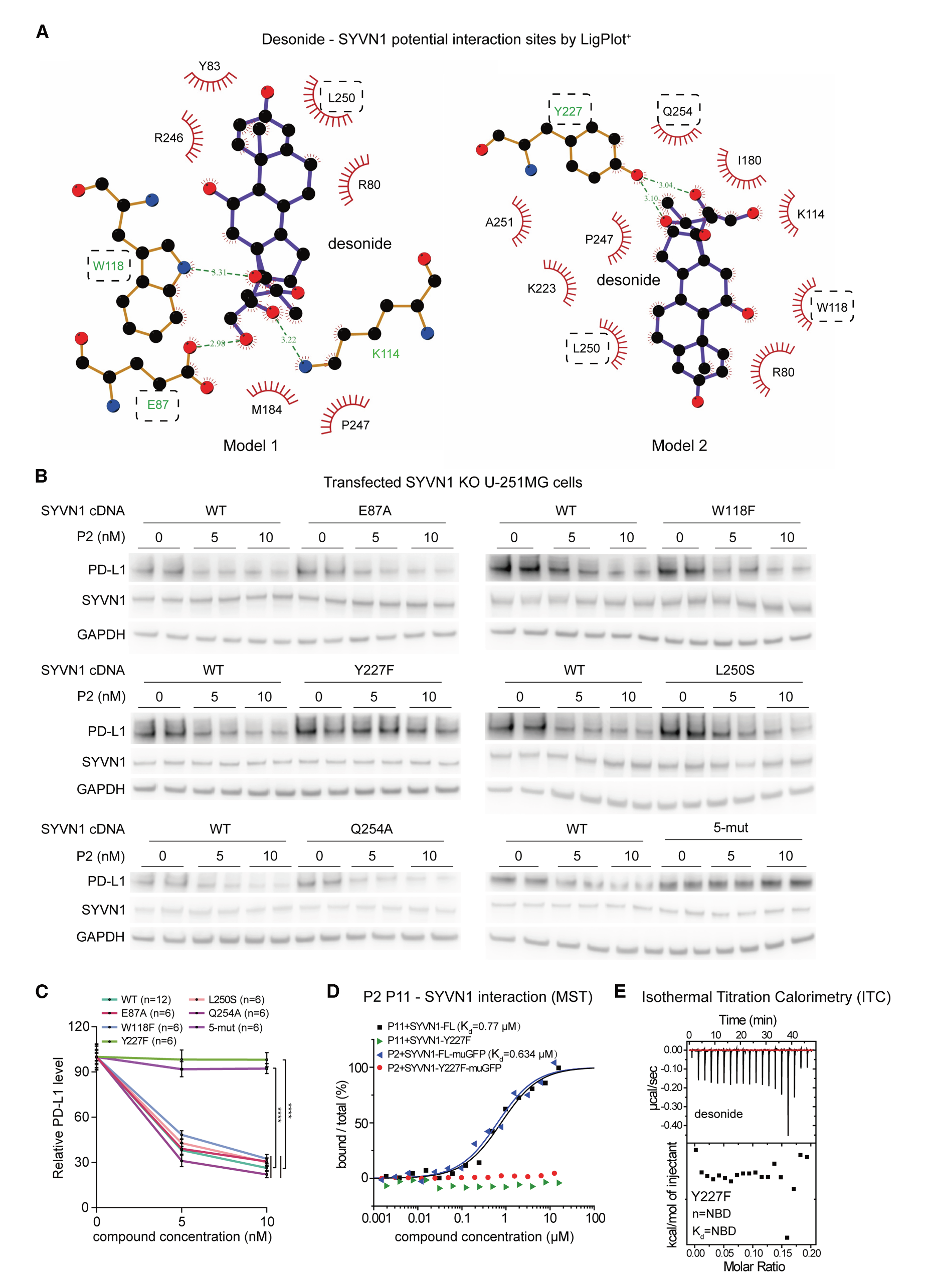
图5. P-ERADECs可能与SYVN1的Y227相互作用以诱导靶向降解
l 蛋白质稳定性分析。用WT或K179R突变hnRNPA1重构的hnRNPA1-KO EnzR细胞,使用蛋白质合成抑制剂环己酰亚胺(CHX)(40微分)处理,可加乳酸或无乳酸(20微分)。西方印迹(A)和hnRNPA1半衰期(B)定量显示乳酸稳定WT,但不稳定K179R hnRNPA1。
l 体内泛素化检测。Flag-hnRNPA1的泛素化在EnzR细胞中低于亲本细胞(C)。乳酸处理(20uM)减少,而氧酸钠(20uM)增加,hnRNPA1泛素化(D)。
l (A) 前两名对接模型的配体-受体相互作用的计算机预测。绿色标记的残基参与氢键,其他残基参与疏水相互作用。突变实验中的突变氨基酸以黑圈标出。
l (B和C) 使用SYVN1敲除的U-251MG细胞,将其转染SYVN1 cDNA(有或没有所示点突变的WT)24小时后,并用P2处理24小时的代表性免疫印迹(B)及其定量(C)。柱状图表示平均值 ± SEM。****p < 0.0001。
l (D) 使用重组纯化蛋白的代表性MST实验结果显示,SYVN1而非Y227F突变体表现出与P-ERADEC (P2或P11)的结合。
l (E) 类似于(D),但使用ITC检测地塞米松的结合。NBD,未检测到结合。另见图S5–S7。
该研究建立了一种新型TPD策略,称为ERADECs,它劫持了ERAD,这是一个尚未在其他TPD中利用的细胞内降解途径。多种P-ERADECs表现出亚纳摩尔级的DC50和超过90%的D max,明显优于传统基于细胞质E3的PD-L1靶向PROTACs,这些传统方法通常表现为大于1 μM的DC50和约60%的D max。这可能是因为PD-L1在ER中折叠,因此对细胞质E3连接酶的可及性有限。膜PD-L1的自然半衰期约为3小时,表明膜中PD-L1部分降解迅速,降低了降解剂提升其降解的空间。总野生型PD-L1的半衰期约为17–18小时,稍长于P-ERADECs发挥作用所需的时间。ERADECs的体内疗效令人期待,表明具有良好的治疗潜力。考虑到用于靶向ERADECs的SYVN1配体(地塞米松)亲和力仅约为μM量级,ERADECs的疗效仍有很大的进一步提升空间。
本研究中使用了中乔新舟的A-375人恶性黑色素瘤细胞专用培养基(货号:ZM0042),NCI-H1975人肺腺癌细胞专用培养基(货号:ZM0395),MDA-MB-231人乳腺癌细胞(货号:ZQ0118),NCI-H1975人肺腺癌细胞(货号:ZQ0395),A375人恶性黑色素瘤细胞(货号:ZQ0042),印证了高端科研对高品质细胞以及专用试剂产品的要求。
中乔新舟提供品种丰富的细胞培养基产品,主要分为基础培养基,细胞系完全培养基,动物原代细胞完全培养基,人原代细胞完全培养基,永生化细胞完全培养基等。该系列产品均由公司技术研发团队历经数年精心设计优化,可保持细胞良好的生长状态。所有产品均有通过严格的质控体系,经过微生物检测、PH值检测、细跑生长验证实验等确保了培养基质量的稳定性。
如果您对我们的产品感兴趣,欢迎联系我们了解更多产品详情。


 上海中乔新舟生物科技有限公司
上海中乔新舟生物科技有限公司